◈ Que signifie matière ?
◈ Quelles sont les propriétés caractéristiques de l'état solide ?
◉ Forme des corps solides :
◉ Volume des corps solides :
◉ Découvrons autres propriétés des corps à l'état solide :
◈ Quelles sont les propriétés caractéristiques de l'état liquide ?
◉ Forme des corps liquides :
◉ Compressibilité des corps liquides :
◉ Surface libre des corps liquides :
◈ Quelles sont les propriétés caractéristiques de l'état gazeux ?
◉ Forme des corps gazeux :
◉ Compressibilité et expansibilité des corps gazeux :
◉ Masse des corps gazeux :
Quelques remarques :
Conclusion générale :
La matière se présente sous plusieurs aspects. Les principaux états de la matière sont : l'état solide, l'état liquide et l'état gazeux.
L'ensemble des corps à l'état liquide et l'état gazeux constitue les fluides.
Les différents états de la matière possèdent des propriétés caractéristiques qui les distinguent les uns des autres.
Quelles sont donc les propriétés caractéristiques de l'état solide, de l'état liquide et de l'état gazeux ?
◈ Quelles sont les propriétés caractéristiques de l'état solide ?
◉ Forme des corps solides :
◉ Volume des corps solides :
◉ Découvrons autres propriétés des corps à l'état solide :
◈ Quelles sont les propriétés caractéristiques de l'état liquide ?
◉ Forme des corps liquides :
◉ Compressibilité des corps liquides :
◉ Surface libre des corps liquides :
◈ Quelles sont les propriétés caractéristiques de l'état gazeux ?
◉ Forme des corps gazeux :
◉ Compressibilité et expansibilité des corps gazeux :
◉ Masse des corps gazeux :
Quelques remarques :
Conclusion générale :
◈ Que signifie matière ?
La matière est l'ensemble de tous les corps et les objets, naturels ou synthétiques, qui nous entourent. La matière est composée d'atomes qui sont eux-mêmes constitués de particules plus petites qui sont les électrons, les protons et les neutrons. Cette matière est caractérisée par une masse.La matière se présente sous plusieurs aspects. Les principaux états de la matière sont : l'état solide, l'état liquide et l'état gazeux.
L'ensemble des corps à l'état liquide et l'état gazeux constitue les fluides.
Les différents états de la matière possèdent des propriétés caractéristiques qui les distinguent les uns des autres.
Quelles sont donc les propriétés caractéristiques de l'état solide, de l'état liquide et de l'état gazeux ?
◈ Quelles sont les propriétés caractéristiques de l'état solide ?
Les corps à l'état solide sont caractérisés par des propriétés telles que la forme propre, l'incompressibilité, ils peuvent être aussi cassants, mous ou élastiques. Dans ce qui suit, nous allons voir en détail toutes ces propriétés.◉ Forme des corps solides :
Prenons comme exemple quelques corps solides tels qu'une bouteille en verre, un bâton en bois et une lame en fer, les trois corps cités sont caractérisés par une forme qui diffère d'un corps à l'autre et qui est propre à chaque corps. Les corps solides sont donc caractérisés par une forme propre.Conclusion : Les solides ont une forme propre.
◉ Volume des corps solides :
Prenons des corps solides quelconques et exerçons sur eux des forces pressantes pour les comprimer ou faire diminuer leur volume. On constate que, même s'ils subissent certaines déformations, les volumes restent toujours les mêmes. Donc, le volume des corps solides ne change pas même si on exerce sur eux des forces.Conclusion : Les solides sont incompressibles.
◉ Découvrons autres propriétés des corps à l'état solide :
Prenons quelques corps solides, exerçons sur eux des forces, puis observons ce qui va se passer ensuite. Ces corps ne réagissent pas de la même façon. On constate que :✦ Certains peuvent se casser, exemple ; la craie, le verre, la règle, etc. On dit que ces corps solides sont cassants.
✦ Certains se déforment sans se casser, exemple ; le plomb, le beurre, etc. On dit que ces corps solides sont mous.
✦ Certains se déforment sans se casser et ils reprennent leur forme initiale lorsque la force n'agit plus. On dit que ces corps solides sont élastiques.
Conclusion : Les corps solides peuvent être cassants, mous ou élastiques.
◈ Quelles sont les propriétés caractéristiques de l'état liquide ?
Dans ce paragraphe, on va aussi mettre en évidence quelques propriétés caractéristiques des corps liquides telles que la forme, le volume, la compressibilité, etc.◉ Forme des corps liquides :
Prenons comme exemple quelques liquides : l'eau, le lait et l'huile. Versons chacun de ces liquides dans un récipient quelconque. On constate que chaque liquide a pris la forme du récipient qui le contient. Donc, le liquide ne possède pas une forme propre puisqu'il prend à chaque fois la forme du récipient où il se trouve, Quelle que soit cette forme du récipient.Conclusion : Les liquides n'ont pas de forme propre.
◉ Compressibilité des corps liquides :
Prenons une quantité d'eau, mettons-la dans une seringue puis exerçons une force sur cette quantité d'eau qui se trouve dans la seringue dans le but de faire diminuer son volume. On constate que l'eau est incompressible. On refait la même expérience avec d'autres liquides (le lait et l'huile). On constate aussi la même chose pour ces deux liquides. Le lait et l'huile sont incompressibles. Alors, le volume d'un liquide ne change pas même si on exerce sur lui une force.Conclusion : Les liquides sont incompressibles.
◉ Surface libre des corps liquides :
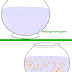
Observons de l'eau dans une bassine. La limite entre l'eau et l'air est appelée surface libre du liquide. Si le liquide est au repos, cette surface libre est plane. Au repos, la surface libre du liquide est toujours horizontale, c'est-à-dire, perpendiculaire à la verticale matérialisé par le fil à plomb.Conclusion : Les liquides possèdent une surface libre toujours horizontale.
◈ Quelles sont les propriétés caractéristiques de l'état gazeux ?
◉ Forme des corps gazeux :
Prenons comme exemple de corps gazeux, l'air que nous respirons, le gaz butane qui est enfermé dans des bouteilles métalliques (le butagaz). Ces gaz, on ne peut ni les toucher ni les manipuler. Ils prennent la forme du récipient dans lequel ils se trouvent.Conclusion : Les gaz n'ont pas de forme propre.
◉ Compressibilité et expansibilité des corps gazeux :
Pour démontrer la compressibilité et l'expansibilité des corps à l'état gazeux, on prend comme exemple de corps gazeux l'air que nous respirons. À l'aide d'une seringue, on aspire une quantité d'air. On ferme le bout de la seringue, puis par l'autre extrémité de la seringue, on exerce une force sur l'air pour diminuer son volume, on constate que le volume de l'air diminue. Si on annule la force exercée sur l'air qui se trouve à l'intérieur de la seringue, le volume de l'air augmente en repoussant l'extrémité de la seringue et il reprend son volume initial. Si on augmente davantage l'espace, l'air occupe tout le volume disponible. On constate donc que le volume de l'air baisse et augmente selon les conditions.Conclusion : Les gaz sont compressibles et expansibles.
◉ Masse des corps gazeux :
Prenons un flacon fermé vide d'air, pesons le, à l'aide d'une balance et marqué sa masse. Ouvrons le flacon, quand l'air pénètre dans le flacon, pesons le, une autre fois. On constate que la masse du flacon ouvert est plus grande que la masse du flacon fermé. L'augmentation de la masse du flacon ouvert est due à la quantité d'air qui a pénétré dans le flacon. On peut déterminer la masse de l'air qui se trouve dans le flacon en faisant la différence entre la masse du flacon ouvert et la masse du flacon fermé. On conclut alors que l'air est pesant.Conclusion : Les gaz sont pesants.
Quelques remarques :
Après avoir déterminé les différentes propriétés caractéristiques des trois états de la matière et qui sont l'état solide, l'état liquide et l'état gazeux, on remarque que dans certains cas, il est difficile de classer quelques substances dans l'un des trois états considérés. Parmi ces substances, on trouve comme exemples :
✤ La farine, le sel fin, la limaille de fer, la fumée, sont constitués de particules solides. Il ne faut pas confondre une fumée formée de fines particules solides avec un gaz. Le brouillard, les nuages, sont formés de particules liquides en suspension dans l'air. Il ne faut pas confondre les nuages, le brouillard, formés d'eau à l'état liquide, avec la vapeur d'eau qui est invisible et formée d'eau à l'état gazeux.
✤ Les huiles coulent plus ou moins facilement. On parle de viscosité des liquides. Le miel coulant est plus visqueux que l'huile de table.
✤ Le dentifrice, la graisse, le verre chauffé, le beurre en été, se trouvent dans un état intermédiaire entre l'état solide et l'état liquide. On parle quelquefois de l'état pâteux.
Conclusion générale :
Nous venons de voir que même les gaz, que l'on ne peut ni les toucher ni les saisir, ont une masse. Donc, on définit la matière de la façon suivante : La matière est tout ce qui est pesant.
La matière existe dans la nature sous trois états : l'état solide, l'état liquide et l'état gazeux.
Chaque état de la matière possède des propriétés caractéristiques qui le distinguent des autres états.
Les propriétés caractéristiques des solides, des liquides et des gaz sont :
✤ Les solides ont une forme propre. Ils ont un volume propre. Ils peuvent être cassants, mous ou élastiques.
✤ Les liquides n'ont pas de forme propre. Ils ont une surface libre toujours horizontale. Ils ont un volume propre. Ils coulent.
✤ Les gaz n'ont pas de forme propre. Ils n'ont pas de volume propre. Ils sont compressibles. Ils sont expansibles. Ils coulent.
🌹🌹🌹 Hi 🙏 Cher(e) visiteur(euse)😍❕ Si vous avez trouvé cet article utile, veuillez le partager avec vos amis pour nous aider à faire connaître NatureLovers❕ Merci d'avance 🙏🌹🌹🌹
À LIRE AUSSI :
1. Quels sont les différents changements d'états physiques de la matière ?
2. Comment séparer les constituants d'un mélange hétérogène ?
3. Notion de mélange, mélange homogène et mélange hétérogène.
4. Notion de corps pur, corps pur simple et corps pur composé.
5. Obtention du corps pur à partir d'un mélange homogène, comment séparer les constituants d'un mélange homogène ?
6. Obtention d'un mélange homogène à partir de corps purs, obtention de solutions.
7. Quels sont les critères de pureté d'un corps ?
8. Que signifie règle de l'octet et règle du duet ?
9. Corps purs à structure atomique : Signification et exemples.
10. Corps purs à structure moléculaire : Signification et exemples.
11. Les molécules de corps simples : Signification et exemples.
12. Les molécules de corps composés : Signification et exemples.
13. L'atome, le constituant élémentaire de la matière.
14. Les électrons d'un atome, leur charge électrique, leur masse et notion de numéro atomique.
15. Le noyau de l'atome, sa masse et sa charge électrique.
À LIRE AUSSI :
1. Quels sont les différents changements d'états physiques de la matière ?
2. Comment séparer les constituants d'un mélange hétérogène ?
3. Notion de mélange, mélange homogène et mélange hétérogène.
4. Notion de corps pur, corps pur simple et corps pur composé.
5. Obtention du corps pur à partir d'un mélange homogène, comment séparer les constituants d'un mélange homogène ?
6. Obtention d'un mélange homogène à partir de corps purs, obtention de solutions.
7. Quels sont les critères de pureté d'un corps ?
8. Que signifie règle de l'octet et règle du duet ?
9. Corps purs à structure atomique : Signification et exemples.
10. Corps purs à structure moléculaire : Signification et exemples.
11. Les molécules de corps simples : Signification et exemples.
12. Les molécules de corps composés : Signification et exemples.
13. L'atome, le constituant élémentaire de la matière.
14. Les électrons d'un atome, leur charge électrique, leur masse et notion de numéro atomique.
15. Le noyau de l'atome, sa masse et sa charge électrique.











Aucun commentaire:
Enregistrer un commentaire